- Биоинформатика и эпигенетика: ключевые открытия, методы и их влияние на современную науку
- Что такое биоинформатика и какую роль она играет в современной науке
- Ключевые направления и инструменты биоинформатики
- Погружение в эпигенетику: что это такое и почему это важно
- Основные механизмы эпигенетической регуляции
- Эпигенетика и болезни: новые горизонты медицины
- Связь между биоинформатикой и эпигенетикой: комплексный подход к анализу данных
- Примеры интегративных проектов и исследований
- Практическое значение и перспективы развития
- Что делать дальше?
Биоинформатика и эпигенетика: ключевые открытия, методы и их влияние на современную науку
В последние десятилетия биология претерпевает революцию, объединяя традиционные лабораторные исследования с передовыми информационными технологиями. Биоинформатика и эпигенетика — это два мощных направления, которые позволяют ученым углубиться в тайны гена, его регуляции и взаимодействия с окружающей средой. За эти годы эти области стали фундаментом для разработки новых методов диагностики, терапии и понимания механизмов развития разных заболеваний.
Давайте разберемся, что же представляет собой биоинформатика, как она связана с эпигенетикой и каким образом эти дисциплины меняют наше представление о жизни на молекулярном уровне. В нашей статье мы расскажем о ключевых понятиях, современных исследованиях, инструментах и перспективах развития, а также о том, как эти области пересекаются и дополняют друг друга.
Что такое биоинформатика и какую роль она играет в современной науке
Биоинформатика, это междисциплинарная область, которая занимается разработкой и применением методов обработки, анализа и интерпретации биологических данных с помощью информационных технологий. Основная цель — превратить огромные массивы молекулярных данных в понятные и практичные знания, которые помогают решать сложные биологические задачи;
Эти данные включают в себя последовательности ДНК, РНК, белков, а также информацию о структуре и функции генов. В силу масштабов и сложности, традиционные методы анализа уже неэффективны, и тут на помощь приходит биоинформатика.
Ключевые направления и инструменты биоинформатики
| Направление | Описание | Примеры инструментов | Применение | Особенности |
|---|---|---|---|---|
| Анализ последовательностей | Обработка ДНК, РНК и белковых последовательностей | BLAST, Bowtie, BWA | Поиск схожих геномных последовательностей, аутосомное картирование | Высокая скорость, точность, автоматизация |
| Геномика и транскриптомика | Исследование структуры геномов и уровней экспрессии генов | DESeq2, Cufflinks | Выявление дифференциальной экспрессии, аннотация генов | Обработка больших данных, визуализация |
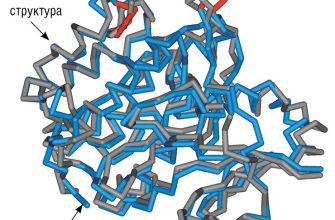
| Анализ структур белков | Моделирование трехмерной структуры белков и взаимодействий | PyMOL, SwissModel | Определение функциональных доменов, разработка лекарств | Интеграция структурных и функциональных данных |
Современная биоинформатика открывает новые горизонты в генетике, молекулярной биологии и медицине, позволяя ученым быстро получать и интерпретировать огромные объемы данных.
Погружение в эпигенетику: что это такое и почему это важно
Эпигенетика — это раздел генетики, изучающий наследуемые изменения в экспрессии генов, которые не связаны с последовательностью ДНК. Эти изменения оказывают влияние на развитие организма, реакцию на факторы окружающей среды, появление заболеваний и процессы старения.
Для многих казалось, что гена — это единственный «код» для жизнедеятельности организма. Однако благодаря открытиям в области эпигенетики стало ясно: на работу генов могут влиять химические метки, расположенные на самих молекулах ДНК или связанных с ними белках. Эти метки регулируют, какие гены активируются или подавляются, что в итоге влияет на клеточные функции и развитие целых систем организма.
Основные механизмы эпигенетической регуляции
- Метилирование ДНК: добавление метильных групп к цитозинам, что обычно подавляет экспрессию гена.
- Модификация гистонов: изменение структуры гистонов, что влияет на доступность ДНК для транскрипции.
- РНК-индуцированная регуляция: использование микроРНК и долгих некодирующих РНК для регулировки генной экспрессии.
Эти механизмы работают совместно, формируя сложную систему регуляции, которая может меняться под воздействием факторов среды, таких как питание, стресс, инфекции и т. д.
Эпигенетика и болезни: новые горизонты медицины
Понимание эпигенетических механизмов открывает новые возможности для диагностики и терапии. Например, изменения в метилировании ДНК наблюдаются при различных видах рака, аутоиммунных заболеваниях, нервных расстройствах. Врачи и ученые используют эти знания для разработки методов раннего обнаружения болезней, а также создания целенаправленных лекарств.
К примеру, использование эпигенетических препаратов (эпигенетических модификаторов) помогает отменить нежелательные метки, нагрузка на гены, что способствует лечению рака и метаболических заболеваний.
Связь между биоинформатикой и эпигенетикой: комплексный подход к анализу данных
Современные исследования не могут обойтись без интеграции биоинформатики и эпигенетики. Специалисты используют алгоритмы для обработки огромных данных о метилировании, посттрансляционных модификациях белков и транскрипционных профилях. Это помогает выявлять новые закономерности и строить модели, объясняющие регуляцию генов на клеточном и системном уровнях.
Например, при исследовании онкологических образований ученым важно анализировать не только ДНК- последовательности, но и эпигенетические метки, чтобы понять механизм распознавания и регуляции раковых клеток.
Примеры интегративных проектов и исследований
- Проект TCGA (The Cancer Genome Atlas) — собирает данные о геноме, транскриптоме, эпигеноме различных типов рака;
- Epigenome RdD — программа, фокусирующаяся на создании карт заболеваний с подробной картой эпигенетических изменений.
- Геном-эпигеномика при исследовании старения и возрастных заболеваний.
Использование таких комплексных данных позволяет понять сложные взаимодействия, которые в будущем помогут создавать персонализированную медицину и новые препараты.
Практическое значение и перспективы развития
Объединив знания в области биоинформатики и эпигенетики, ученые смогут не только лучше понять причины заболеваний, но и разработать новые методы их лечения и профилактики. В будущем нас ожидает появление более точных диагностических маркеров, терапий, направленных на изменение эпигенетических меток, и технологий, позволяющих управлять генами на молекулярном уровне.
Рассмотрим основные перспективы:
- Персонализированная медицина: лечение с учетом индивидуальных генетических и эпигенетических особенностей.
- Редактирование эпигенетических меток: возможность управлять регуляцией генов без изменения их последовательности.
- Молекулярные биомаркеры: ранняя диагностика и прогнозирование заболеваний по эпигенетическим изменениями.
- Интеграция данных: объединение геномных, транскриптомных и эпигенетических данных для комплексного анализа.
Что делать дальше?
Если вас заинтересовала эта тема, стоит учитывать, что современные технологии активно развиваются, и специалисты в области биоинформатики и эпигенетики востребованы как никогда. Обучение программированию, статистике, молекулярной биологии и медицине — ключ к будущему, в котором мы сможем не только лучше понимать жизнь, но и лечить болезни с точностью до молекулы.
Вопрос: Почему интеграция биоинформатики и эпигенетики так важна для современной медицины?
Ответ: Интеграция этих областей позволяет комплексно анализировать генетическую и эпигенетическую информацию, что способствует созданию более точных диагнозов, эффективных методов лечения и профилактики заболеваний. Это важно, поскольку здоровье человека зависит не только от последовательности его генов, но и от их регуляции, которая определяется эпигенетическими механизмами.
Подробнее
| Геномика | Эпигенетика | Биоинформатика | Модификации ДНК | Метки гистонов |
| Исследование геномных последовательностей | Изучение изменений в регуляции генов | Обработка данных и моделирование | Добавление или удаление метильных групп | Регуляция доступа к ДНК |