- Использование глубокого обучения для прогнозирования эффекта мутаций
- Что такое мутации и почему их предсказание важно
- Основы глубокого обучения в predicts эффект мутаций
- Ключевые этапы использования глубокого обучения для прогнозирования эффекта мутаций
- Обзор популярных архитектур нейронных сетей для анализа мутаций
- Практические кейсы и достижения в использовании глубокого обучения
- Преимущества и ограничения современных подходов
- Будущее прогнозирования эффектов мутаций с помощью глубокого обучения
Использование глубокого обучения для прогнозирования эффекта мутаций
В современном мире биотехнологий и медицины одним из крупнейших вызовов становится понимание того, как именно генетические изменения – мутации – влияют на здоровье организма и развитие различных заболеваний․ Современные методы анализа генетической информации требуют не только глубоких знаний, но и мощных инструментов для обработки огромных объемов данных․ На стыке биологии и искусственного интеллекта возникает направление, посвященное использованию глубокого обучения для прогнозирования последствий мутаций․
Кроме того, что такие технологии помогают предсказывать влияние конкретных мутаций на структуру и функцию белков, они также открывают новые горизонты в диагностике и терапии․ В этой статье мы подробно разберем, как современные алгоритмы глубокого обучения используются для анализа мутаций, почему это важно и какие перспективы открывают перед наукой и медициной․
Что такое мутации и почему их предсказание важно
Мутации, это изменения в последовательности ДНК, которые могут возникать спонтанно или под воздействием внешних факторов․ Обычно каждая мутация несет с собой определенные последствия для организма: она может быть безвредной, ухудшать работу клетки или, наоборот, приносить пользу․ В медицине особенно важно уметь точно предсказывать последствия мутаций, чтобы диагностировать наследственные заболевания, определить риск развития рака или разработать эффективные методы лечения․
В нынешней практике многие мутации критичны для формирования различных болезней, поэтому разработка инструментов для их анализа стала приоритетом․ Традиционные эксперименты требуют много времени и ресурсов, тогда как с помощью алгоритмов машинного обучения можно значительно ускорить и упростить этот процесс․
Основы глубокого обучения в predicts эффект мутаций
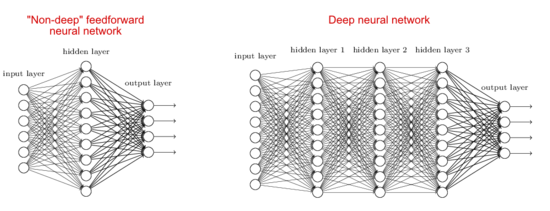
Глубокое обучение — это направление машинного обучения, использующее нейронные сети с множеством слоев для обучения сложных паттернов․ В контексте анализа генетической информации такие модели позволяют выявлять взаимосвязи между последовательностью ДНК и функциями белков, а также предсказывать последствия мутаций․
На практике, чтобы предсказать эффект мутации, нейронная сеть обучается на обширных наборах данных, где известны последовательности и их функциональные последствия․ После тренировки модель способна оценить новые, ранее невиданные мутации, основываясь на усвоенных закономерностях․
Ключевые этапы использования глубокого обучения для прогнозирования эффекта мутаций
- Сбор и подготовка данных: Получение последовательностей ДНК, белков, а также информации о функциях и патологиях, связанных с мутациями․
- Обучение модели: Использование архитектур типа сверточных нейронных сетей (CNN), рекуррентных нейронных сетей (RNN) или трансформеров для распознавания паттернов․
- Валидация и тестирование: Проверка модели на новых данных для оценки ее точности и надежности․
- Прогнозирование: Применение обученной модели к новым мутациям для предсказания их последствий․
Обзор популярных архитектур нейронных сетей для анализа мутаций
| Архитектура | Плюсы | Минусы | Примеры использования | Рекомендуемые задачи |
|---|---|---|---|---|
| Convolutional Neural Networks (CNN) | Хорошо работают с последовательностями, выявляют локальные паттерны | Могут требовать много ресурсов, сложная настройка | Определение вредных мутаций в белках | Классификация изменений воздействия мутаций |
| Recurrent Neural Networks (RNN) | Обрабатывают последовательные данные, моделируют контекст | Медленно обучаются, проблема затухания градиента | Анализ последовательностей ДНК | Прогнозирование функции мутаций |
| Transformers | Обработка длинных зависимостей, высокая точность | Высокие требования к вычислительным ресурсам | Модели типа AlphaFold | Предсказание структуры белков и эффектов мутаций |
Практические кейсы и достижения в использовании глубокого обучения
Один из наиболее ярких примеров — использование AlphaFold от DeepMind, который совершил революцию в предсказании трехмерной структуры белка․ В результате стало возможным понять, как конкретные мутации могут изменить структуру и, следовательно, функцию белка․ Это значительно помогает в разработке новых лекарств и терапии наследственных заболеваний․
Еще один пример — применение моделей для оценки вредности новых вариаций ДНК․ Такие системы охотно используют генетические лаборатории и компании по секвенированию для быстрого скрининга огромных массивов данных и выявления потенциальных опасных мутаций․
Преимущества и ограничения современных подходов
- Преимущества: Быстрый анализ, высокая точность, возможность автоматизации, масштабируемость․
- Ограничения: Требовательность к вычислительным ресурсам, необходимость в больших объемах качественных данных, риск переобучения модели․
Будущее прогнозирования эффектов мутаций с помощью глубокого обучения
Технологии не стоят на месте, и будущее предсказания эффектов мутаций выглядит очень перспективным․ Уже сейчас активно развиваются модели, способные не только определять вредность или благоприятность мутаций, но и предсказывать их влияние на структуру белков, взаимодействия и даже терапевтическую эффективность․
В ближайшие годы ожидается появление интегрированных платформ, использующих разные алгоритмы для комплексного анализа генетической информации․ Также важным направлением станет развитие методов explainable AI – систем, которые помимо предсказаний дают объяснения по сути, что особенно важно для медицинских целей․
Вопрос: Можно ли полностью положиться на алгоритмы глубокого обучения при определении риска генетических заболеваний?
Ответ: Хотя современные модели показывают отличные результаты и значительно ускоряют диагностику, они не могут полностью заменить врачу или генетику․ Важно помнить, что алгоритмы являются помощниками, которые предоставляют дополнительные данные и оценки․ Финальное решение должно базироваться на комплексном анализе, включающем генетическую информацию, клинические данные и профессиональное мнение специалиста․
Подробнее
| аналитика генетических данных | машинное обучение в медицине | предсказание эффектов мутаций | глубокое обучение и биоинформатика | нейронные сети для анализа ДНК |
| структура белка и мутации | генетические алгоритмы и машинное обучение | предсказание наследственных болезней | In silico анализ мутаций | Анализ вариантов и интерпретация данных |