- Методы аннотирования генома для клинического применения: путь к персонализированной медицине
- Что такое аннотирование генома? Обзор понятия
- Ключевые методы аннотирования генома в клинике
- Аппаратное и программное обеспечение для предобработки данных
- Выравнивание последовательностей и нахождение вариантов
- Выделение функциональных элементов
- Актуализация баз данных и аннотирование функций
- Анализ вариантов и их клиническая интерпретация
- Клиническое значение аннотирования генома
- Трансформация клинической практики
- Практическое применение: кейсы из работы медицинских центров
- Будущее аннотирования генома в клинике: тренды и вызовы
Методы аннотирования генома для клинического применения: путь к персонализированной медицине
В современную эпоху геномика занимает ключевую роль в медицине‚ предоставляя уникальные возможности для точной диагностики‚ прогноза и терапии различных заболеваний. Одним из важнейших этапов работы с геномными данными является
методика аннотирования генома — процесс определения функций генов‚ их взаимосвязей‚ механизмов действия и роли в организме человека. Мы вместе рассмотрим‚ как методы аннотирования применяются в клинической практике и что они дают для развития персонализированной медицины.
Что такое аннотирование генома? Обзор понятия
Аннотирование генома — это процесс присвоения биологической функции и идентификации генетического материала на основе полученных данных секвенирования. Он включает в себя определение расположения генов‚ выявление регуляторных элементов‚ кодирующих последовательностей и вариантов. В клинической практике это важно потому‚ что понимание функции генов позволяет диагностировать наследственные заболевания‚ выявлять предрасположенность и разрабатывать таргетные терапии.
Проще говоря‚ когда мы говорим о аннотировании генома‚ речь идет об ответе на вопросы:
- Где находится ген и что он делает?
- Какие мутации в нем обнаружены и как они влияют на здоровье?
- Какие регуляторные участки расположены поблизости и регулируют его работу?
Ключевые методы аннотирования генома в клинике
Сегодня в клинической геномике используются разнообразные подходы и инструменты для максимально точного и быстрого аннотирования. Рассмотрим основные из них:
Аппаратное и программное обеспечение для предобработки данных
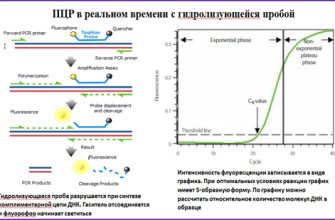
Перед началом аннотирования необходимо обеспечить качество данных секвенирования. Для этого используют инструменты‚ такие как FastQC и Trimmomatic‚ которые позволяют проверить качество чтений и удалить низкокачественные фрагменты.
Выравнивание последовательностей и нахождение вариантов
Затем проводится выравнивание читов к референсному геному с помощью программ вроде BWA или Bowtie2. В ходе этого этапа выявляются различия — мутации‚ вставки‚ делеции‚ которые далее анализируются для определения клинической значимости.
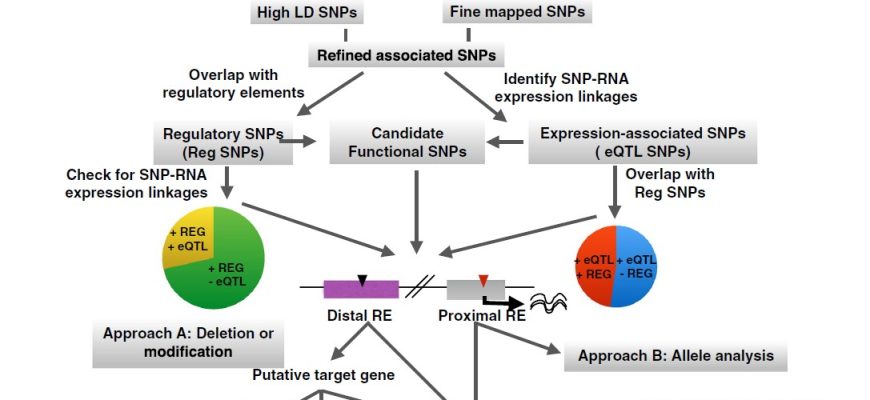
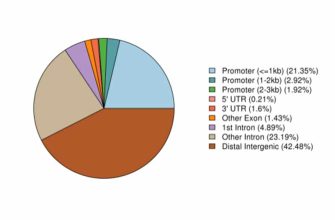
Выделение функциональных элементов
Ключевым моментом является идентификация генов‚ регуляторных элементов‚ потенциальных сайтв сплайсинга. Для этого применяют базы данных и алгоритмы типа GENSCAN или Augustus для предсказания генов и их структуры.
Актуализация баз данных и аннотирование функций
Важнейшей частью является сопоставление выявленных последовательностей с уже известными данными из GENCODE‚ RefSeq‚ Ensembl. Эти ресурсы предоставляют информацию о функциях вариантов‚ экспрессии и известной патологии.
Анализ вариантов и их клиническая интерпретация
В клинической практике особое значение имеет интерпретация вариантов. Для этого используют базы данных‚ такие как ClinVar‚ HGMD‚ и программы типа ANNOVAR. Они помогают определить‚ является ли мутация патогенной или гипопатогенной.
Клиническое значение аннотирования генома
Используемые методы позволяют идентифицировать мутации‚ связанные с наследственными заболеваниями‚ онкологическими процессами‚ метаболическими нарушениями и множеством других патологий. Это открывает новые горизонты в:
- Диагностике редких болезней
- Определении предрасположенности к онкозаболеваниям
- Выборе персональной терапии
- Мониторинге эффективности лечения
Трансформация клинической практики
Объединение данных аннотирования с технологиями машинного обучения‚ искусственного интеллекта и автоматизации делает возможным автоматическую интерпретацию сотен тысяч вариантов за короткое время. Это позволяет подходить к каждому пациенту максимально индивидуально и повысить эффективность лечения.
Практическое применение: кейсы из работы медицинских центров
В наших клиниках опыт показывает‚ что успешное аннотирование генома позволяет:
- Обнаружить скрытые причины редких генетических заболеваний у пациентов
- Предсказать риск развития определенных болезней еще до появления симптомов
- Разработать индивидуальные программы профилактики и лечения
Специалисты отмечают‚ что правильная интерпретация данных требует междисциплинарного подхода и постоянного обновления баз знаний.
Будущее аннотирования генома в клинике: тренды и вызовы
Ожидается‚ что в ближайшие годы развитие методов аннотирования будет способствовать повышению точности и скорости диагностики. Ведущие тренды включают:
- Интеграцию геномных данных с протеомикой и метаболомикой
- Разработку более точных алгоритмов предсказания патогенности
- Создание глобальных платформ для обмена и анализа данных
Однако перед нами стоят вызовы: необходимость стандартизации методов‚ обеспечения конфиденциальности данных и обучения специалистов новым технологиям.
Общаясь с пациентами‚ важно понимать‚ что современная медицина — это не только лечение симптомов‚ но и глубокое понимание генетичес-ких механизмов. Методы аннотирования генома — это мост между достигнутыми научными знаниями и практическим применением. Они позволяют нам быть на шаг впереди в борьбе с болезнями и предоставляют уникальную возможность для каждого человека стать участником персонализированной медицины.
"Знание о методах аннотирования генома дает возможность не только лучше понять здоровье и болезни‚ но и выбрать наиболее эффективное лечение‚ ориентированное именно на вас."
Подробнее
| геномное аннотирование | методы секвенирования в медицине | клиническая геномика | генетические мутации | персонализированная медицина |
| информационные системы в геномике | аннотирование вариантов | генетическая диагностика | клонирование гена | методы биоинформатики |
| научные разработки в геномике | геннотерапия | генетическая предрасположенность | биоинформатические базы данных | причины генетических заболеваний |