- Прогнозирование структуры белков и его роль в определении предрасположенности к заболеваниям
- Что такое структура белка и почему она важна?
- Зачем нужно прогнозирование структуры белка?
- Техники прогнозирования структуры белка
- Модели на основе гомологии
- Аб initio методы
- Методы на основе машинного обучения
- Роль искусственного интеллекта в прогнозировании структур белков
- Применение прогнозирования структуры белков в медицине и предрасположенности к заболеваниям
- Диагностика наследственных болезней
- Выбор терапевтических методов
- Примеры современных исследований и кейсы
- Кейс 1: Разработка вакцин против коронавируса
- Кейс 2: Исследование мутаций при онкологических заболеваниях
- Будущее прогнозирования структур белков
Прогнозирование структуры белков и его роль в определении предрасположенности к заболеваниям
Когда мы задумываемся о сложности человеческого организма, одним из самых удивительных и многообразных элементов являются белки. Эти молекулы выполняют бесчисленное количество функций — от поддержки иммунной системы до выполнения строительных работ на клеточном уровне. Но как узнать, каким именно образом белок принимает свою 3D-структуру? Почему это так важно для медицины и предрасположенности к тем или иным заболеваниям? В этой статье мы подробно расскажем о технике прогнозирования структуры белков, о том, как этот процесс помогает понять риски развития заболеваний и какие современные методы используют ученые в этой области.
Что такое структура белка и почему она важна?
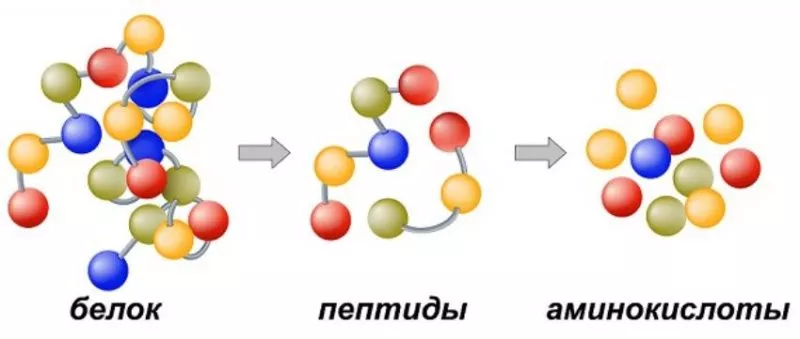
Белок — это цепочка аминокислот, которая, складываясь по определенному принципу, превращается в сложную трехмерную структуру. Именно от этой структуры зависит его функция: будь то фермент, антитело или структурный компонент клетки. Каждая часть белка, от первичной цепочки до окончательной третичной и четвертичной структуры, играет роль в его деятельности.
Например, небольшие изменения в правильной форме белка могут привести к серьезным нарушениям в физиологических процессах. Это особенно важно при изучении наследственных заболеваний или реакций на лекарства. Поэтому понимание структуры белка помогает не только понять его функции, но и предсказать, как мутации могут влиять на организм в целом.
Зачем нужно прогнозирование структуры белка?
Благодаря прогнозированию структуры белков ученые получают уникальные возможности:
- Диагностика генетических заболеваний: выявление мутаций, которые могут нарушать структуру и функцию белка.
- Разработка лекарств: создание таргетных препаратов, которые связываются с определенными участками белка.
- Изучение патогенеза: понимание, как измененные белки вызывают болезни.
- Персонализированная медицина: подбор терапии, основанный на индивидуальном генетическом составе и структурных особенностях белков.
В большинстве случаев, экспериментальные методы определения структуры — такие как рентгеновская кристаллография, крио-ЭМ и ядерный магнитный резонанс — требуют много времени и ресурсов. Поэтому развитие методов компьютерного моделирования стало ключом к быстрому и недорогому анализу новых белков.
Техники прогнозирования структуры белка
Современные подходы к предсказанию структуры белков можно условно разделить на две большие категории: экспериментальные и вычислительные. В настоящее время мы сосредотачиваемся главным образом на вычислительных методах, которые позволяют построить модели на базе последовательности аминокислот.
Модели на основе гомологии
Этот метод использует существующие данные о структурах похожих белков для предсказания формы исследуемого. Если у нас есть известная структура белка-близнеца, мы можем мысленно "скопировать" её, модифицируя под наш конкретный случай. Такой подход называется моделирование по гомологии. Он быстрый и часто очень точный, если близкий аналог существует.
Аб initio методы
Этот подход основан на первых принципах и использует физические модели взаимодействия аминокислот. Он менее точен и требует огромных вычислительных ресурсов, но способен предсказать структуру даже для новых, уникальных белков без известных аналогов.
Методы на основе машинного обучения
Появившиеся последние годы алгоритмы, такие как AlphaFold от Google, произвели революцию в области прогнозирования. Они используют огромные массивы данных, чтобы обучить нейронные сети предсказывать структуру белка с высокой точностью, значительно опередив традиционные методы.
Роль искусственного интеллекта в прогнозировании структур белков
Искусственный интеллект и машинное обучение сегодня становятся ключевыми инструментами молекулярной биологии. Алгоритмы способствуют быстрому и точному предсказанию 3D-структур, что в свою очередь помогает определить возможные генетические предрасположенности к заболеваниям.
Например, алгоритмы типа AlphaFold позволяет моделировать сложные белковые структуры, которые раньше требовали месяцы работы в лаборатории. Это особенно важно для исследований редких заболеваний или новых вирусов, таких как коронавирус, где быстрый анализ структуры белка позволяет своевременно создать эффективные лекарства и вакцины.
Применение прогнозирования структуры белков в медицине и предрасположенности к заболеваниям
Рассмотрим практическое использование прогнозных моделей на примере диагностики наследственных заболеваний и определения риска развития конкретных патологий.
Диагностика наследственных болезней
Многие наследственные болезни связаны с мутациями в генах, кодирующих важные белки. Предсказание их структуры помогает понять, как именно эти мутации мешают белку выполнять его функции. В случае с мутациями, которые вызывают изменение третичной структуры, разрабатываются стратегии коррекции или лечения, основанные на конкретных дефектах.
Выбор терапевтических методов
Зная точные изменения в структуре белка, врачи могут рекомендовать препараты, которые лучше связываются с измененным белком или способствуют его правильной ориентации. Это позволяет создавать персонализированные методики лечения, что значительно повышает эффективность терапии.
Примеры современных исследований и кейсы
Давайте рассмотрим несколько ярких примеров, как прогнозирование структуры белков помогает в практической медицине и научных открытиях.
Кейс 1: Разработка вакцин против коронавируса
Использование алгоритмов предсказания структуры белков вируса SARS-CoV-2 позволило быстро определить ключевые участки спайкового белка, что стало основой для разработки эффективных vaccine candidates. Это значительно ускорило процессы, приводящие к появлению вакцин.
Кейс 2: Исследование мутаций при онкологических заболеваниях
Моделирование структур белков, вовлеченных в развитие рака (например, рецепторных белков), выявило изменения, вызывающие их аномальную активность. Эти данные помогают разрабатывать таргетные терапевтические препараты и прогнозировать риск развития онкологии у пациентов.
Будущее прогнозирования структур белков
Технологии продолжают развиваться, открытия идут быстрым темпом. В ближайшие годы ожидается расширение возможностей автоматизированных систем предсказания и интеграция их в клиническую практику. Чем больше данных и мощнее модели, тем выше шанс обнаружить новые связи между структурой белка и его ролью в болезнях.
Также перспективно развитие методов в области персонализированной медицины, где комплекс генетической информации позволяет создавать индивидуальные планы лечения, основанные на предсказании структурных изменений белков у конкретного человека.
Итак, прогнозирование структуры белков — это не просто научный интерес, а важнейший инструмент современной медицины. Благодаря развитию вычислительных технологий и методов искусственного интеллекта мы можем быстрее и точнее исследовать молекулярные механизмы заболеваний, что открывает новые горизонты в диагностике, лечении и профилактике. В перспективе эти исследования сделают медицину более персонализированной и эффективной, помогая каждому из нас вести здоровье под контролем.
Вопрос: Какая роль современных технологий в прогнозировании структуры белков и как это влияет на медицину будущего?
Ответ: Современные технологии, такие как алгоритмы машинного обучения и искусственный интеллект, позволяют моделировать белковые структуры с высокой точностью и скоростью. Это существенно ускоряет диагностику наследственных и приобретенных заболеваний, помогает создавать таргетные лекарства и разрабатывать персонализированные методы терапии. В будущем эти инструменты станут неотъемлемой частью медицины, делая её более точной, быстрой и доступной для каждого человека.
Подробнее
| как предсказать структуру белка | прогнозирование белков и заболевания | использование AI в биологии | методы моделирования белков | новые технологии в молекулярной биологии |
| примеры структурных белков | разработка лекарств на основе моделей | машинное обучение в медицине | какие есть программы для моделирования | будущее персонализированной медицины |
| роля гомологичного моделирования | структура и функции белка | AlphaFold и его возможности | как работают ab initio модели | клинические применения прогноза белков |
| разработка вакцин будущего | генетические мутации и риск заболеваний | прогнозирование мутаций | научные кейсы применения | перспективы развития исследований |
| методы экспериментального подтверждения | структурные базы данных | использование структур в терапии | проблемы точности моделирования | этика и безопасность в генетических исследованиях |